1979. godine mladi patolog Robin Warren primijetio je spiralnu bakteriju u biotičkim uzorcima sluznice želuca bolesnika s gastritisom te je pretpostavio da postoji povezanost između te, do tada nepoznate bakterije, i bolesti.
1981. godine pridružio mu se gastroenterolog Barry Marshall, s kojim je nastavio istraživati povezanost bakterije i gastritisa. U to su vrijeme njihove tvrdnje smatrane kontroverznima jer se općenito vjerovalo da je gastritis uzrokovan stresom, ljutom hranom i želučanom kiselinom. Kako bi dokazao svoju hipotezu, Marshall se sam namjerno zarazio bakterijom te obolio od gastritisa.
1989. godine bakterija je dobila naziv Helicobacter pylori.
Tijekom godina nedvojbeno je potvrđena povezanost između H. pylori i gastritisa, peptičkog ulkusa te tumora želuca. Ovo otkriće omogućilo je uspješno liječenje, a za svoje revolucionarno postignuće, Marshall i Warren dobili su Nobelovu nagradu za medicinu 2005. godine.

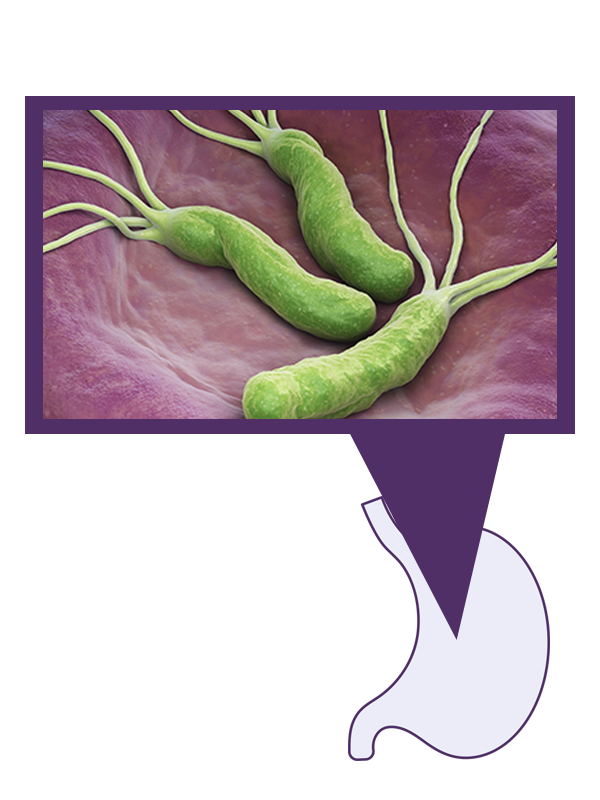
Želudac je organ koji, lučenjem enzima i kiseline, sudjeluje u probavi, ali nas također štiti od patogena koje unosimo u organizam kroz usta. Uz iznimku našeg želučanog mikrobioma, većina mikroorganizama ne može dugotrajno živjeti u kiselim uvjetima (pH 1.5-3.5). Helicobacter pylori je jedna od rijetkih iznimki.
Sluznica želuca (epitel) osim kiseline i probavnih enzima luči i sluz (mukus) koja oblaže unutrašnjost želuca te štiti stanice od kiseline. H. pylori živi unutar mukoznog sloja. Ova bakterija ima sposobnost lučenja ureaze, enzima koji razgrađuje ureu u amonijak, stvarajući alkalne uvjete u svom neposrednom okolišu, što joj omogućuje preživljavanje. Dodatno, građena je tako da posjeduje do šest flagela (izdanaka nalik bičevima) koji joj omogućuju kretanje. Iako se najčešće nalazi u dijelu želuca koji nazivamo antrum, može se detektirati i u drugim dijelovima želuca. Ponekad se bakterija može naći i u dvanaesniku, a iznimno u jednjaku ili usnoj šupljini.
Na strane mikroorganizme organizam reagira upalom. Iako upala djelomično oštećuje naša tkiva, istovremeno uništava patogene s kojima se tijelo bori. Nakon što se organizam izbori s infekcijom, oštećena tkiva počinju cijeliti te obnavljaju svoju strukturu i funkciju. Međutim, Helicobacter pylori ima sposobnost odupiranja našim urođenim mehanizmima obrane, a njena prisutnost uzrokuje kroničnu upalu želuca – gastritis. Dugotrajna prisutnost H. pylori u želucu održava upalu i istovremeno inhibira prirodne procese obnove stanica. Zbog toga se stanice želuca strukturno mijenjaju, nakupljaju mutacije DNA koje se ne mogu popraviti, te gube sposobnost obavljanja svoje primarne funkcije. Kronična upala i nemogućnost stanica domaćina da poprave svoju DNA dovodi do akumulacije mutacija, što u konačnici može dovesti do razvoja karcinoma.
Medicinskim rječnikom, proces preobrazbe stanica uzrokovan infekcijom H. pylori naziva se Correa kaskada, a uključuje upalu, atrofiju, intestinalnu metaplaziju i u konačnici adenokarcinom. Stadiji atrofije, intestinalne metaplazije i displazije smatraju se prekanceroznim stanjem.
Želučani mikrobiom odnosi se na skupinu mikroorganizama (bakterija, virusa, gljivica) koji prirodno žive u želucu. Iako je želudac vrlo kiselo okruženje, određene vrste bakterija mogu preživjeti i obavljati važne funkcije, poput pomaganja u probavi i održavanju zdravlja želuca.
Ravnoteža tih mikroorganizama je ključna za normalno funkcioniranje probavnog sustava, a poremećaji mikrobioma mogu dovesti do raznih bolesti. Prisustvo H. Pylori narušava zdravi mikrobiom želuca.

Načini širenja
Helicobacter pylori prenosi se s čovjeka na čovjeka kontaktom sa slinom ili probavnim izlučevinama, direktno ili indirektno (oro-oralni ili fekalno-oralni prijenos).
Infekcija se najčešće događa u lošim higijenskim uvjetima, primjerice nepranjem ruku, konzumacijom kontaminirane hrane ili vode, dijeljenjem hrane i pića, ali i izravnim kontaktom, poput poljubaca.
Infekcija najčešće nastupa u dječjoj dobi, do 12. godine života
Rizici ponovne infekcije
Uzimajući u obzir način prijenosa bakterije, zaraza Helicobacter pylori najčešće se događa u dječjoj dobi, no zaraza, kao i reinfekcija u odrasloj dobi, također su moguće.
Naš organizam, naime, proizvodi protutijela usmjerena protiv bakterije, koja se mogu detektirati u krvi godinama nakon preboljene infekcije. Međutim, ta protutijela nisu zaštitna (ne neutraliziraju bakteriju).
Što je niža prevalencija infekcije u populaciji u kojoj živimo i što su bolji higijenski i sanitarni uvjeti, to su manje šanse za reinfekciju.
* Prevalencija – učestalost neke bolesti u određenoj populaciji
* Reinfekcije – ponovna zaraza istim infektivnim uzročnikom

H. pylori gastritis: Zarazna bolest
2015. godine, H. pylori gastritis službeno je proglašen zaraznom bolešću te je preporučeno liječenje svih zaraženih osoba, neovisno o tome imaju li simptome ili ne.
Helicobacter pylori uvijek uzrokuje gastritis (upalu želuca), koji dugo vremena može biti bez simptoma (asimptomatska bolest).
Komplikacije infekcije H. pylori najčešće nastupaju nakon dugogodišnje infekcije i uključuju:
Osim toga, ako nisu utvrđeni drugi uzroci, dokazano je da se sideropenična anemija, idiopatska trombocitopenična purpura i manjak vitamina B12 mogu pripisati H. pylori infekciji.
H. pylori-inducirani gastritis najčešće se klinički očituje dispepsijom.
Dispepsija je skupni naziv za niz nespecifičnih simptoma gornjeg probavnog sustava, uključujući blagu bol, pečenje i nelagodu u gornjem dijelu trbuha, blagu mučninu i nadutost.
Peptički ulkus se najčešće klinički očituje bolovima u gornjem dijelu trbuha, mučninom, povraćanjem, ranom sitosti, a ako prokrvari stolica postaje crna (katranasta) i proljevasta. Takva stolica naziva se melena.
Naš organizam funkcionira na principu pozitivnih i negativnih povratnih sprega. Kada nečega nedostaje, aktiviraju se mehanizmi koji potiču proizvodnju, a kad ga ima previše, ti mehanizmi inhibiraju daljnju proizvodnju.
Helicobacter pylori najčešće se nalazi u antrumu želuca, gdje uzrokuje upalu i oštećenje stanica koje inhibiraju lučenje kiseline (antralni gastritis). To narušava prirodni mehanizam povratne sprege, što dovodi do pojačanog lučenja kiseline. Zbog toga bolesnici mogu osjetiti olakšanje simptoma dispepsije prilikom uzimanja inhibitora protonske pumpe, čak i ako bakterija nije eradicirana.
Bakterija može živjeti i u tijelu (lat. corpusu) želuca, gdje oštećuje stanice koje luče kiselinu. To se najčešće događa kod osoba koje dugotrajno uzimaju inhibitore protonske pumpe i istovremeno su zaražene H. pylori. Nakon uspješne eradikacije bakterije, funkcija stanica se može oporaviti, što kod nekih bolesnika može uzrokovati prolazne refluksne tegobe.
U nekim slučajevima, prisutnost H. pylori ne utječe značajno na lučenje kiseline.
Testiranje na Helicobacter pylori moguće je neinvazivnim i invazivnim testovima. Obje metode su podjednako točne.
Neinvazivna testiranja uključuju:
Invazivno testiranje uključuje gastroskopiju i uzimanje uzorka sluznice za analizu. Na uzorku sluznice moguće je provesti brzi test na H. pylori – brzi ureaza test, ili uzorak može biti poslan na patohistološku analizu, gdje se bakterija može prikazati pod mikroskopom.

Urea izdisajni test: Smatra se zlatnim standardom neinvazivnog testiranja.
Osjetljivost testa: 95-98%, specifičnost testa: 95-100%
H. pylori proizvodi enzim ureazu, koji razgrađuje ureu na amonijak i CO2.
Testiranje započinje uzimanjem uzorka izdaha (puhanjem u vrećicu), nakon čega osoba popije tekućinu koja sadrži ureu. Ako je H. pylori prisutna u želucu, proizvodi se CO2, koji se apsorbira u krvi. Analizom drugog uzorka izdaha, koncentracija CO2 u izdahnutom zraku bit će veća nego u prvom uzorku.
Osoba daje uzorak stolice u kojem se detektiraju proteini specifični za bakteriju, izlučeni stolicom.
Osjetljivost testa: 90-95%, specifičnost testa: 94-98%
Budući da sve H. pylori bakterije nisu strukturno jednake, postoji mogućnost da test zasnovan na detekciji antigena bude negativan ako je osoba zaražena sojem iz drugog geografskog područja, primjerice ako je osoba zaražena u Aziji, a testira se na u jednoj od zapadnih zemalja.

Kada se zarazimo H. pylori bakterijom, naš organizam proizvodi protutijela usmjerena protiv bakterije, koja se mogu detektirati u uzorku krvi. Međutim, protutijela mogu biti prisutna godinama nakon eradikacije bakterije, stoga nisu marker isključivo aktivne infekcije, već i prethodnog kontakta s bakterijom. U kliničkoj praksi, ako je serološki test pozitivan, potrebno je provesti dodatna testiranja kako bi se potvrdila ili isključila aktivna infekcija.
Osjetljivost testa je sposobnost testa da prepozna stvarno bolesne osobe.
Specifičnost testa je sposobnost testa da prepozna stvarno zdrave osobe.
Primjer: Ako test ima osjetljivost od 98%, to znači da će 98 od 100 zaraženih osoba biti ispravno identificirano kao bolesne, dok će 2 osobe biti lažno negativne. Ako test ima specifičnost 98%, to znači da će 98 od 100 testiranih osoba biti ispravno identificirane kao zdrave, dok će 2 osobe biti lažno pozitivne.
Rijetko koji test koji se koristi u medicini je 100% točan. Za dijagnozu bolesti koristimo testove koji imaju najpovoljniji omjer osjetljivosti i specifičnosti.
Kada se zakazuje termin za neinvazivno testiranje (urea izdisajni test, određivanje H. Pylori antigena u stolici), liječnik će vas upozoriti da mora proći barem 14 dana od zadnje doze inhibitora protonske pumpe te barem 4 tjedna od zadnje doze antibiotika i bizmuta.
Inhibitori protonske pumpe smanjuju lučenje želučane kiseline. U manje kiselom okruženju broj bakterija privremeno se smanjuje, a bakterija postaje manje aktivna, tj. proizvodi manje količine enzima ureaze. Uporaba različitih antibiotika (i onih propisanih u svrhu koja nije eradikacija H. pylori) također može privremeno smanjiti broj bakterija i/ili izravno inhibirati lučenje ureaze, zbog čega je manja vjerojatnost da će prisutnost bakterije biti otkrivena. Sličnim mehanizmom djeluje i bizmut, lijek s djelomično antibakterijskim učinkom.

Kao i ostali živi organizmi, bakterija se bori za preživljavanje te se mutacijama prilagođava okolišu. Postoje različiti sojevi Helicobacter pylori, uglavnom specifični za određena geografska područja. U nekim dijelovima svijeta, H. pylori je agresivnija (virulentnija), dok u drugim područjima rjeđe dovodi do ozbiljnih komplikacija.
Virulentni (agresivni) sojevi H. pylori između ostalog proizvode CagA protein, koji se inkorporira u stanice želuca te mijenja njihovu funkciju i strukturu, te virulentni oblik VacA toksina, koji izravno oštećuje epitelne stanice domaćina.
* CagA i VacA nazivaju se virulentnim faktorima H. pylori. CagA i virulentna forma VacA toksina nisu jedini prepoznati virulentni faktori, no smatraju se najvažnijima.
Iako je moguće testirati na prisutnost virulentnih faktora, takva testiranja se ne provode u rutinskoj kliničkoj praksi, jer su testovi značajno skuplji i ne mijenjaju plan liječenja – svaka infekcija H. pylori treba biti eradicirana.
Virulentni sojevi češće dovode do komplikacija, ali virulentni potencijal bakterije nije jedini faktor koji utječe na nepovoljan klinički tijek.
U modernom svijetu, zbog česte i široke primjene antibiotika, sve više bakterija razvija otpornost na lijekove, što predstavlja ozbiljan globalni problem. Tijekom proteklih 40 godina zabilježen je značajan porast rezistencije H. pylori na dostupne terapije.
Kako bi se odredio najbolji protokol liječenja, lokalna stručna društva provode istraživanja o rezistenciji bakterija i prikupljaju podatke o uspješnosti liječenja na lokalnoj razini. Na temelju tih podataka kreiraju se protokoli prve i druge linije liječenja.
Moguće je testirati osjetljivost bakterije na antibiotike na individualnoj razini, no za to je potrebna gastroskopija. Osim toga, ti su testovi tehnički zahtjevni, a činjenica da je bakterija osjetljiva na određeni antibiotik u laboratorijskim uvjetima (in vitro) ne znači nužno da će terapija biti uspješna u praksi.
Individualno kreiranje terapijskog protokola je moguće, no velike studije su pokazale da je stopa eradikacije bakterije podjednaka kod osoba liječenih prema lokalnim protokolima i onih kod kojih su terapije individualno prilagođene.
Nakon provedene terapije potrebno je ponoviti testiranje kako bi se utvrdila uspješnost liječenja.
Važno je da se testiranje provede s dovoljnim vremenskim odmakom od zadnje doze antibiotika, inhibitora protonske pumpe i bizmuta kako bi se izbjegli lažno negativni nalazi.
Na gastroskopiju i testiranje osjetljivosti na pojedine antibiotike odlučujemo se kod osoba kod kojih eradikacija bakterije nije postignuta ni nakon druge linije liječenja preporučene prema lokalnim smjernicama.
* Eradikacija: potpuno uništenje uzročnika zarazne bolesti
Trenutno, u europskim zemljama protokol prve linije liječenja naziva se četverostruka terapija s bizmutom i uključuje:
Ako pojedina sastavnica preporučenog protokola nije lokalno dostupna, zamjenjuje se lijekom koji je dokazano učinkovit. S obzirom na to da tetraciklin u Hrvatskoj nije registriran za liječenje H. pylori, u terapijskom protokolu koristi se amoksicilin.
Alternative četverostrukoj terapiji bizmutom u prvoj liniji liječenja su:
Trajanje terapije je 14 dana.
(Napomena: Za osobe alergične na penicilin postoji alternativna prva linija liječenja.)
Cilj liječenja je eradikacija bakterije, odnosno uništenje uzročnika zarazne bolesti.
Kombinacijom dva različita antibiotika smanjuje se vjerojatnost razvoja otpornosti bakterije. Također, budući da antibiotici djeluju različitim mehanizmima, veća je šansa za uspješnu eradikaciju infekcije.
Protokoli prve linije liječenja imaju uspješnost eradikacije H. pylori veću od 90%.
Uloga probiotika se mnogo istraživala, no za sada nema dokaza da liječe H. pylori infekciju. Međutim, uz probiotike bolja je podnošljivost antibiotika, što poboljšava suradljivost bolesnika i time povećava uspješnost liječenja.
Prva linija liječenja učinkovita je u više od 90% slučajeva. Nakon provedene terapije, liječnik vas upućuje na testiranje radi potvrde eradikacije. Potvrda eradikacije najčešće se izvodi neinvazivnim testovima – urea izdisajnim testom ili testom na H. pylori antigen u stolici. Ako je nalaz pozitivan, propisat će se druga linija liječenja. Nakon provedene terapije, ponovno se testira uspješnost liječenja. U slučaju ponovnog pozitivnog nalaza, liječnik vas upućuje na gastroskopiju tijekom koje se uzimaju biopsije sluznice želuca radi kultivacije bakterije i testiranja osjetljivosti na antibiotike, na temelju čega se dizajnira individualna terapija.
U malom broju slučajeva, nijedna linija liječenja nije učinkovita. Te osobe smatraju se visokorizičnima za razvoj komplikacija, uključujući ulkusnu bolest i tumor. Zbog toga im se preporučuje cjeloživotna terapija inhibitorima protonske pumpe i redovite preventivne gastroskopije (svake 3 godine).
H. pylori infekcija uvijek uzrokuje upalu želuca (gastritis), koja može biti bez simptoma ili uzrokovati neugodne tegobe kao što su nelagoda, pečenje i bol u gornjem dijelu trbuha. Nadalje, upala može dovesti do razvoja ulkusa (čira) na želucu i/ili dvanaesniku, koji mogu krvariti, a u rijetkim slučajevima, puknuti (perforirati).
Rizik krvarenja iz ulkusa želuca je 4,8 puta veći kod osoba koje uzimaju nesteroidne antireumatike, a ako su te osobe zaražene H. pylori, rizik krvarenja je 6,1 puta veći.
Liječenjem infekcije omogućuje se zacjeljivanje sluznice želuca i sprječava razvoj komplikacija, posebno u prisutnosti drugih rizičnih čimbenika.
Kronična H. pylori infekcija uzrokuje strukturne i funkcionalne promjene u stanicama želuca, koje u konačnici mogu dovesti do razvoja karcinoma želuca. Stanice se postupno mijenjaju tijekom vremena i prolaze kroz prekancerozne stadije, koje nazivamo atrofija, intestinalna metaplazija i displazija. Liječenjem infekcije sprečava se daljnje napredovanje staničnih promjena, a moguća je i djelomična reverzija, odnosno oporavak strukture i funkcije.
Adenokarcinom je najčešći oblik raka želuca, a u oko 90% slučajeva povezuje se s infekcijom bakterijom Helicobacter pylori. H. pylori također uzrokuje MALT-limfom, a prva linija liječenja ove zloćudne bolesti je upravo eradikacija H. pylori. Brojna istraživanja dokazala su da eradikacija bakterije značajno smanjuje incidenciju raka želuca, a jedan od najilustrativnijih primjera dolazi s otoka Matsu, arhipelaga od 36 otoka smještenih uz istočnu obalu Kine, u blizini Tajvana.
Na Matsu otocima, 2004. godine pokrenut je projekt eradikacije H. pylori za sve stanovnike starije od 30 godina. Tijekom 14 godina trajanja projekta, 85,5% ciljne populacije testirano je urea izdisajnim testom, a 93,3% pozitivnih na infekciju odlučilo se za liječenje. U usporedbi s incidencijom adenokarcinoma želuca prije provođenja projekta, tijekom trajanja inicijative zabilježeno je smanjenje učestalosti ove maligne bolesti za 53%. Nije zabilježen razvoj otpornosti bakterije na antibiotike korištene u liječenju.
Eradikacija Helicobacter pylori ne znači da ne postoji šansa za razvoj adenokarcinoma želuca. Dugogodišnja infekcija H. pylori može uzrokovati postupne promjene stanica sluznice želuca. Procjenjuje se da oko 10% zaraženih osoba do 50. godine života razvije uznapredovale (prekancerozne) promjene sluznice, poput atrofičnog gastritisa, intestinalne metaplazije ili displazije. Iako su te promjene djelomično reverzibilne, kod uznapredovalih stadija atrofičnog gastritisa rizik od razvoja adenokarcinoma ostaje povišen, čak i nakon eradikacije bakterije.
Osim infekcije H. pylori, važni rizični čimbenici za razvoj karcinoma kardije (gornjeg dijela želuca) uključuju pretilost i gastroezofagealnu refluksnu bolest (GERB), kronične bolesti čija prevalencija raste zbog nezdravog zapadnog načina života. U manjem broju slučajeva, adenokarcinom želuca može biti genetski uvjetovan.
Prevencija karcinoma želuca je najučinkovitija ako se liječenje provodi u mlađoj dobi, prije nego što nastupe prekancerozne promjene. Eradikacija bakterije kod osoba koje planiraju obitelj ili su tek zasnovale obitelj također smanjuje šanse zaraze kod potomaka, jer je infekcija najčešća u djetinjstvu kroz kontakt sa zaraženim članovima obitelji.
* Eradikacija: potpuno uništenje uzročnika zarazne bolesti
Malfertheiner P, Megraud F, Rokkas T, et al. Management of Helicobacter pylori infection: the Maastricht VI/Florence consensus report. Gut. 2022 Aug 8. doi:10.1136/gutjnl-2022-327745.
Lordick F, Carneiro F, Cascinu S, et al. Gastric cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2022 Oct;33(10):1005–1020.
Sugano K, Tack J, Kuipers EJ, et al. Kyoto global consensus report on Helicobacter pylori gastritis. Gut. 2015 Sep;64(9):1353–1367.
Arnold M, Ferlay J, van Berge Henegouwen MI, Soerjomataram I. Global burden of oesophageal and gastric cancer by histology and subsite in 2018. Gut. 2020;69(9):1564-1571.
Chiang TH, Chang WJ, Chen SL, et al. Mass eradication of Helicobacter pylori to reduce gastric cancer incidence and mortality: a long-term cohort study on Matsu Islands. Gut. 2021 Feb;70(2):243-250.
Espada M, Nyssen OP, Gisbert JP. Empirical versus susceptibility- guided treatment ofHelicobacter pylori infection: a meta- analysis. United European Gastroenterol J 2020;8:251
Zhu X, Zhao Y, Zhu C, et al. Rapid detection of cagA-positive Helicobacter pylori based on duplex recombinase aided amplification combined with lateral flow dipstick assay. Diagn Microbiol Infect Dis. 2022;103(1):115661.
Chiang TH, Chang WJ, Chen SL, et al. Mass eradication of Helicobacter pylori to reduce gastric cancer incidence and mortality: a long-term cohort study on Matsu Islands. Gut. 2021;70(2):243-250.

TOGAS (Towards Gastric Cancer Screening Implementation in the European Union) projekt je usmjeren na razvoj učinkovitih metoda u borbi protiv zloćudnih tumora želuca.
Sve zainteresirane osobe u dobi od 30 do 34 godine, koje nisu ranije liječene zbog H. pylori infekcije, mogu se informirati i prijaviti putem e-maila:




Ovaj je projekt primio sredstva Europske unije u sklopu programa EU4 Health, Grant Agreement broj 101101252.
Financirano od strane Europske unije. Stavovi i mišljenja izneseni ovdje pripadaju isključivo autorima te ne predstavljanju nužno stavove i mišljenja Europske unije ili Europske izvršne agencije za zdravlje i digitalno gospodarstvo (eng. European Health and Digital Executive Agency, HaDEA). Sukladno tome niti Europska unija niti izvršna agencija ne mogu biti odgovorni sa izneseni sadržaj.
© Copyright by KBC Zagreb
Ova web stranica koristi tehnologije kao što su kolačići kako bi omogućila osnovne funkcije stranice, kao i za analitiku, personalizaciju i ciljano oglašavanje. Možete promijeniti postavke u bilo kojem trenutku ili prihvatiti zadane postavke.