U hrvatskom jeziku riječi “tumor” ili “novotvorina” označavaju svaku izraslinu koja nije dio normalne građe tijela.
Ljudski organizam građen je od različitih organa, organi od različitih tkiva, a tkiva od različitih stanica. Genetski kod svake stanice u tijelu može se promijeniti, što može uzrokovati funkcionalne promjene u stanici. Ako se stanica počne ubrzano dijeliti, nastaje tumor (novotvorina).
Tumori (novotvorine) dijele se na dobroćudne (benigne) i zloćudne (maligne).
Kod dobroćudnih tumora, stanice tvore mase koje obično dosegnu određenu veličinu i ne utječu značajno na funkciju tkiva i organa. No, ako narastu do kritične veličine, mogu pritiskati okolna tkiva i organe, uzrokujući tegobe, što nazivamo “efektom mase”.
S druge strane, kada se stanice nekontrolirano dijele, govorimo o zloćudnim tumorima. Kako će se zloćudni tumor ponašati i kakve su mogućnosti liječenja, ovisi o vrsti stanice iz koje je nastao.
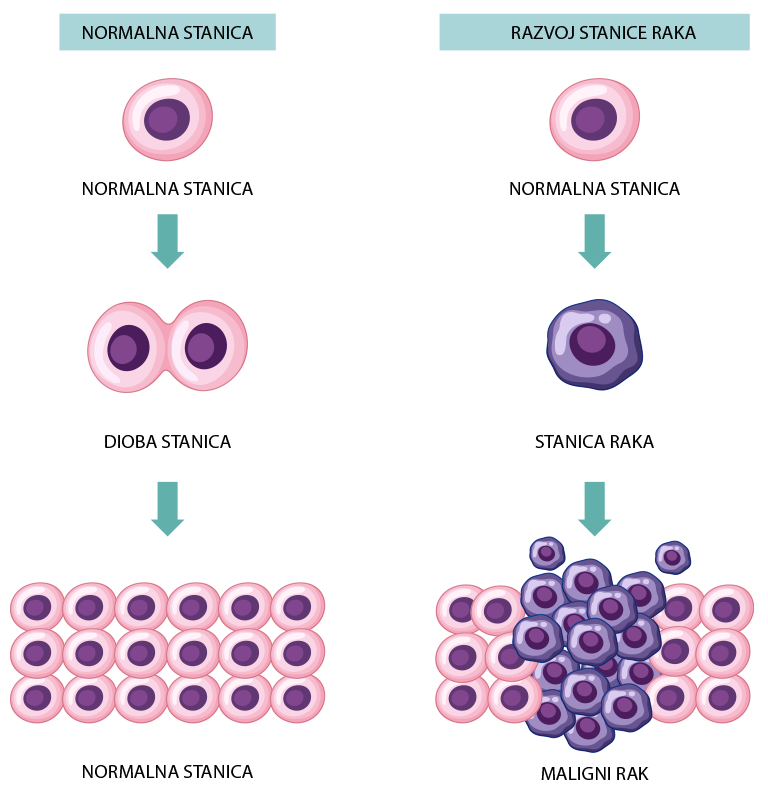
Nazivi tumora, bilo dobroćudnih ili zloćudnih, određuju se prema stanici iz koje potječu, tj. stanici koja je doživjela genetske promjene i počela nekontrolirano dijeliti. U hrvatskom kolokvijalnom jeziku jeziku, skupni naziv za sve zloćudne tumore, neovisno od koje stanice potječu, je ‘’rak’’.
Stanice koje oblažu stijenke krvnih žila te tjelesne površine koje su u kontaktu s vanjskim okolišem, poput kože, sluznice probavnog, respiratornog i urogenitalnog sustava, nazivaju se epitelnim stanicama. Tumori koji nastaju iz ovih stanica nazivaju se karcinomima.
Postoji više vrsta epitelnih stanica koje obavljaju različite funkcije. Ako se specijalizirana epitelna stanica, poput žlijezdane stanice koja izlučuje tvari poput sluzi (mukusa), hormona, enzima i drugih sekreta, počne nekontrolirano dijeliti, govorimo o adenokarcinomu.
U 90% slučajeva, zloćudni tumor želuca je adenokarcinom. Rjeđi oblici tumora uključuju gastrointestinalni stromalni tumor (GIST), limfome poput MALT-limfoma i difuznog velikostaničnog B-limfoma želuca, te neuroendokrine tumore. Osim primarnih tumora želuca, kod osoba koje boluju od drugih zloćudnih bolesti moguće moguća je i pojava presadnica (metastaza) u stijenku želuca.
Rizični čimbenici za razvoj adenokarcinoma želuca
Glavni uzrok adenokarcinoma želuca i MALT-limfoma je infekcija bakterijom Helicobacter pylori.
Drugi rizični čimbenici za razvoj adenokarcinoma želuca uključuju prekomjernu konzumaciju alkohola, pušenje, visoki unos soli, konzumaciju crvenog i procesiranog mesa kao i nedovoljan unos svježeg voća i povrća. Za adenokarcinom spoja želuca i jednjaka, dodatni rizični čimbenici su gastroezofagealna refluksna bolest (GERB) i pretilost.
Sporadičan i nasljedni adenokarcinom
Adenokarcinom želuca u 90% slučajeva je sporadičan (javlja se slučajno, bez jasne obiteljske predispozicije), dok se u 10% slučajeva može utvrditi obiteljska sklonost prema ovoj bolesti. U 1-3% slučajeva moguće je identificirati genetsku mutaciju koja predisponira nastanku tumora, tada govorimo o nasljednim karcinomima.
Kod osoba s definiranom genetskom predispozicijom, eradikacija H. pylori smanjuje rizik razvoja adenokarcinoma, ali te osobe i dalje ostaju visoko rizične te se preporučuje intenzivno endoskopsko praćenje, a u rijetkim slučajevima i preventivno uklanjanje želuca (gastrektomija).
* Eradikacija: potpuno uništenje uzročnika zarazne bolesti
U Hrvatskoj se rizik razvoja karcinoma želuca procjenjuje na temelju testiranja na Helicobacter pylori, obiteljske anamneze i nalaza gastroskopije.
Dodatna laboratorijska testiranja, poput testova na pepsinogen, gastrin i protutijela, liječnik propisuje ako postoje indikacije, uzimajući u obzir ostale laboratorijske nalaze i simptome pacijenta.


Testiranje na H. pylori
Prisutnost infekcije povezana je s povećanim rizikom od razvoja adenocarcinoma želuca I MALT-limfoma.

Obiteljska anamneza
Genetska predispozicija može igrati ulogu u razvoju tumora želuca.

Gastroskopija
Osobe s prekanceroznim promjenama sluznice želuca (atrofični gastritis, intestinalna metaplazija, displazija) pod povišenim su rizikom adenocarcinoma želuca. Te promjene moguće je dokazati samo patohistološkom analizom uzoraka sluznice želuca dobivenih prilikom gastroskopije.

Testovi krvi (proenzimi i hormoni)
Kod osoba s dugotrajnim gastritisom i prekancerozno promijenjene stanice želuca ne obavljaju adekvatno svoju funkciju zbog čega je povišeno ili smanjeno lučenje hormona i proenzima. Smanjene koncentracije pepsinogena, odnosno povišene koncentracije gastrina u krvi mogu biti znak prekanecroznih promjena stanica sluznice želuca.

Testovi krvi (protutijela)
Protutijela na parietalne stanice i/ili na intrinzični faktor mogu ukazivati na autoimuni gastritis, stanje koje nosi povišen rizik tumora želuca.
Učestalost bolesti u određenoj populaciji u definiranom vremenskom periodu izražava se pojmovima incidencija i prevalencija.
Incidencija označava broj novodijagnosticiranih slučajeva (broj novooboljelih) u određenom vremenskom periodu.
Prevalencija označava ukupan broj oboljelih osoba, neovisno o tome je li dijagnoza postavljena prije ili tijekom definiranog vremenskog razdoblja.
Kada se prikupljaju epidemiološki podaci o učestalosti malignih bolesti u populciji, najčešće se bilježi učestalost bolesti prema sijelu npr. rak želuca, rak debelog crijeva, rak pluća…a rjeđe imamo dostupne podatke o učestalosti podtipova. Prilikom interpretacije podataka o učestalosti raka želuca trebamo imati na umu da se 90% slučajeva raka želuca radi o adenokarcinomu.
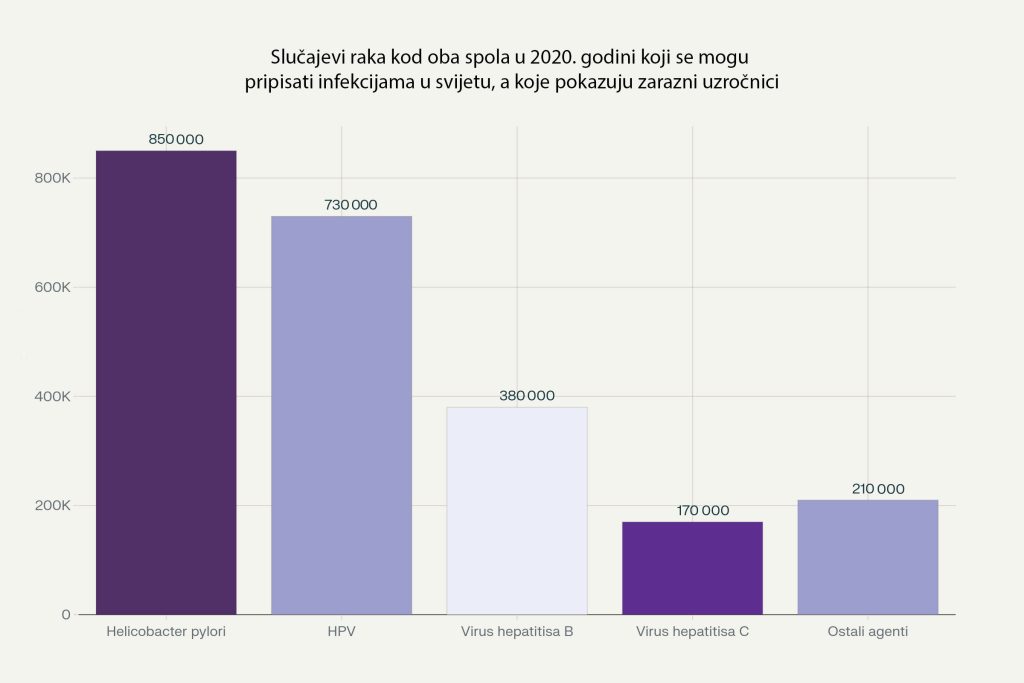
Godine 2018., 13% novo dijagnosticiranih tumora u svijetu pripisano je infektivnim uzročnicima, a Helicobacter pylori bio je vodeći infektivni uzrok tumora.
Incidencija tumora povezanih s infekcijama varira od zemlje do zemlje, ovisno o prevalenciji dotične infekcije u toj regiji.
Epstein-Barr virus (EBV), najpoznatiji kao uzročnik infektivne mononukleoze, iako najčešće uzrokuje asimptomatske infekcije u djetinjstvu, također se povezuje s adenokarcinomom želuca. Ipak, infekcija H. pylori daleko je češći uzrok raka želuca u usporedbi s EBV-om.
Na globalnoj razini, najčešći infektivni uzroci malignih bolesti su:
1. Helicobacter pylori – adenokarcinom želuca i MALT-limfom.
2. Humani papiloma virus (HPV) – karcinom vrata maternice
3. Hepatitis B virus (HBV) – hepatocelularni karcinom jetre.
4. Hepatitis C virus (HCV) – hepatocelularni karcinom jetre.
Adenokarcinom želuca je agresivna bolest koja u ranijim fazama može biti bez simptoma. Prvi simptom tumora želuca najčešće je dispepsija.
Dispepsija je skupni naziv za niz nespecifičnih simptoma koji ukazuju na bolest gornjeg dijela probavnog sustava, a uključuju: blagu bol, pečenje i/ili nelagodu u gornjem dijelu trbuha, blagu mučninu i nadutost. Simptomi dispepsije nisu specifični samo za tumor želuca, već se često javljaju i kod dobroćudnih bolesti želuca (gastritisa), bolesti žučnog sustava i gušterače.
U uznapredovalim stadijima simptomi i znakovi tumora želuca mogu uključivati:
Navedene simtpome nazivamo ‘’alarmantnim’’ simptomima.
Osobe s alarmantnim simptomima (npr. rana sitost, neobjašnjivi gubitak težine, krv u stolici, anemija) i/ili pozitivnom obiteljskom anamnezom, bez obzira na dob, kao i osobe starije od 45-50 godina s dispeptičnim tegobama, trebaju biti upućene na gastroskopiju. Također, gastroskopija je indicirana kod osoba mlađih od 45-50 godina kod kojih tegobe perzistiraju i nakon provedene eradikacijske terapije.
Definitivna dijagnoza adenokarcinoma želuca može se postaviti samo ezofagogastroduodenoskopijom (EGDS), pri kojoj se uzimaju bioptički uzorci sluznice želuca. Tumori želuca različitog podrijetla, poput karcinoma i limfoma, često izgledaju slično pri vizualnom pregledu, zbog čega je patohistološka analiza ključna za daljnje planiranje dijagnostike i liječenja.
Tumor želuca najčešće izgleda kao ulkus (čir), no ako se tijekom gastroskopije otkrije ulkus želuca, a biopsije ne pokažu prisutnost malignih stanica, propisuje se terapija, nakon čega se planira kontrolna gastroskopija. Ako ulkus zacijeli, to je obično znak dobroćudnog peptičkog ulkusa.
Ako se patohistološkom analizom potvrdi dijagnoza adenokarcinoma želuca, liječnik će bolesnika uputiti na CT (kompjuteriziranu tomografiju) radi utvrđivanja proširenosti bolesti i određivanja stadija tumora.
Kod tumora u najranijim stadijima, može se koristiti endoskopski ultrazvuk za precizniju procjenu zahvaćenosti stijenke želuca i okolnih limfnih čvorova.
U određenim slučajevima, liječnik može zatražiti PET-CT, iako se ta pretraga ne provodi rutinski. Naime, hoće li se adenokarcinom vidjeti na PET pretrazi, ovisi o njegovim biološkim i patohistološkim karakteristikama. Kod nekih vrsta tumora, PET može dati lažno negativan rezultat.
U slučajevima kada se proširenost adenokarcinoma želuca ne može precizno utvrditi pomoću CT-a, EUS-a ili PET-a, liječnik može preporučiti dijagnostički operativni zahvat, poznat kao eksplorativna laparotomija.
Ezofagogastroduodenoskopija (EGDS) je medicinski pregled kojim liječnik pomoću tankog, savitljivog uređaja s kamerom na vrhu (zvanog gastroskop) pregledava unutrašnjost jednjaka, želuca i dvanaesnika (prvi dio tankog crijeva). Tijekom pregleda, uređaj se uvodi kroz usta, prolazi kroz grlo i spušta se u želudac. Liječnik na ekranu prati snimku i može odmah vidjeti eventualne promjene ili oštećenja sluznice. Ako je potrebno, može uzeti uzorke tkiva (biopsiju) za dodatnu analizu.
Kolokvijalno, umjesto punog naziva ‘’ezofagogastroduodenoskopija’’ najčešće koristimo riječ ‘’gastroskopija’’.
Patohistološka analiza je postupak kojim se detaljno ispituje uzorak tkiva pod mikroskopom kako bi se utvrdilo postoje li promjene ili bolesti u stanicama, poput tumora. Uzorak tkiva uzima se obično tijekom operacije ili biopsije, a zatim se posebno obrađuje i boji da bi liječnik mogao vidjeti detalje unutar stanica.
Ovaj pregled omogućuje liječniku da vidi kako tkivo izgleda na mikroskopskoj razini, otkrivajući promjene u stanicama koje bi mogle ukazivati na bolest, poput upale, infekcije ili tumora. Patohistološka analiza ključna je za točnu dijagnozu mnogih bolesti jer pruža informacije koje se ne mogu dobiti drugim metodama pregleda.
Na primjer, ako postoji sumnja na tumor, patohistološka analiza može potvrditi prisutnost tumorskih stanica i odrediti tip tumora, što je važno za planiranje daljnjeg liječenja.
U najranijim fazama, kada tumor zahvaća samo dio stijenke želuca, adenokarcinom se može liječiti endoskopskim putem ili kirurškom resekcijom dijela ili cijelog želuca, ovisno o lokaciji tumora i njegovim mikroskopskim karakteristikama (biološkom ponašanju).
Ako tumor zahvaća cijelu stijenku želuca i širi se u okolno tkivo, oboljele osobe prvo primaju neoadjuvantnu kemoterapiju (prije operacije), a zatim slijedi radikalna kirurška resekcija te adjuvantna kemoterapija (nakon operacije).
U slučaju proširene (metastatske) bolesti, bolesnici se najčešće liječe kemoterapijom i/ili imunoterapijom. U određenim situacijama, onkolog može odlučiti o primjeni radioterapije kao dijela liječenja.
Kada govorimo o preživljenju kod malignih bolesti, često koristimo pojam petogodišnjeg preživljenja. To znači da, ako osoba pet godina nakon liječenja nema znakova povrata bolesti, smatra se izliječenom.
Petogodišnje preživljenje kod najranijeg stadija adenokarcinoma želuca iznosi između 70 i 90%, dok je kod proširene bolesti (metastatskog stadija) petogodišnje preživljenje manje od 5%.
Općenito, preživljenje kod malignih bolesti ovisi o samoj prirodi tumora, odnosno o njegovom agresivnom potencijalu, ali i o općem stanju bolesnika. Osobe koje su u dobrom fizičkom zdravlju i imaju očuvanu mišićnu masu imaju bolje izglede za preživljenje nego pacijenti koji su u lošijem općem stanju ili imaju pridružene kronične bolesti.

Malfertheiner P, Megraud F, Rokkas T, et al. Management of Helicobacter pylori infection: the Maastricht VI/Florence consensus report. Gut. 2022 Aug 8. doi:10.1136/gutjnl-2022-327745.
Lordick F, Carneiro F, Cascinu S, et al. Gastric cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2022 Oct;33(10):1005–1020.
Sugano K, Tack J, Kuipers EJ, et al. Kyoto global consensus report on Helicobacter pylori gastritis. Gut. 2015 Sep;64(9):1353–1367.
Chen YC, Malfertheiner P, Yu HT, et al. Global prevalence of Helicobacter pylori infection and incidence of gastric cancer between 1980 and 2022. Gastroenterology. 2024 Apr;166(4):605–619.
de Martel C, Georges D, Bray F, et al. Global burden of cancer attributable to infections in 2018: a worldwide incidence analysis. Lancet Glob Health. 2020 Feb;8(2):e180–e190.
Emami MH, Ataie-Khorasgani M, Jafari-Pozve N. Diagnostic value of alarm symptoms for upper GI malignancy in patients referred to GI clinic: A 7 years cross sectional study. J Res Med Sci. 2017 Jun 21;22:76.
Schiller MP, Wilkerson PM. Gastric neoplasms. Surgery (Oxford). 2017;35(11):635–643.

TOGAS (Towards Gastric Cancer Screening Implementation in the European Union) projekt je usmjeren na razvoj učinkovitih metoda u borbi protiv zloćudnih tumora želuca.
Sve zainteresirane osobe u dobi od 30 do 34 godine, koje nisu ranije liječene zbog H. pylori infekcije, mogu se informirati i prijaviti putem e-maila:




Ovaj je projekt primio sredstva Europske unije u sklopu programa EU4 Health, Grant Agreement broj 101101252.
Financirano od strane Europske unije. Stavovi i mišljenja izneseni ovdje pripadaju isključivo autorima te ne predstavljanju nužno stavove i mišljenja Europske unije ili Europske izvršne agencije za zdravlje i digitalno gospodarstvo (eng. European Health and Digital Executive Agency, HaDEA). Sukladno tome niti Europska unija niti izvršna agencija ne mogu biti odgovorni sa izneseni sadržaj.
© Copyright by KBC Zagreb
Ova web stranica koristi tehnologije kao što su kolačići kako bi omogućila osnovne funkcije stranice, kao i za analitiku, personalizaciju i ciljano oglašavanje. Možete promijeniti postavke u bilo kojem trenutku ili prihvatiti zadane postavke.